Cuáles son las dos vacunas chinas que están cerca de probarse en la Argentina
Miércoles 19 de
Agosto 2020
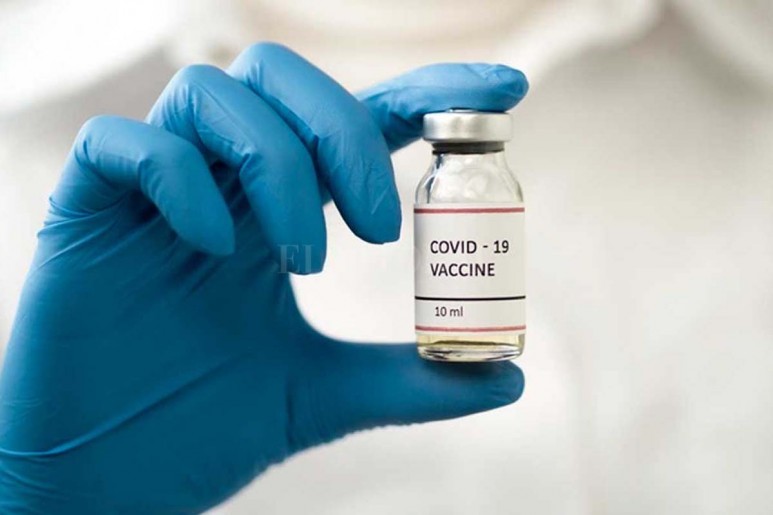
De sumarse, como todo indica, las dos desarrolladas en el gigante asiático, se estudiarían en el país la de los laboratorios Sinopharm y CanSino. Fuentes oficiales aseguraron a Infobae que "todavía no está confirmado", aunque es muy probable que así ocurra.
El gobierno Nacional anunciaría pronto el comienzo de pruebas en el país de dos vacunas china, la de Sinopharm y la de CanSino, y sumarían cuatro los desarrollos de este tipo en la Argentina, además del de la Universidad de Oxford y AstraZeneca, y el de Pfizer, cuyas pruebas ya se están realizando en el Hospital Militar Central.
La importancia de estos acuerdos radica en que facilitará el acceso a dosis en el futuro.
Sin embargo, según pudo saber Infobae de parte de fuentes calificadas del Ministerio de Salud, “falta la confirmación oficial” de esos acuerdos. En la misma línea se manifestó consultado por este medio el médico infectólogo Pedro Cahn, quien aseguró que “todavía está en discusión” (que se realicen las pruebas en el país).
“En 48 horas va a haber novedades sobre las vacunas chinas”, aseveró por su parte, el ministro de Salud, Ginés González García, en declaraciones televisivas. “Estamos trabajando intensamente con China. Nosotros queremos mucho a los proveedores de vacunas; queremos que haya disponibilidad para todos los argentinos a partir de acuerdos con proveedores, sobre todo quienes están en la punta del desarrollo”, agregó.
Ayer se dio a conocer que Liu Jingzhen, el presidente de la empresa estatal China National Biotec Group, parte de la farmacéutica Sinopharm, aseguró que la vacuna contra el coronavirus en la que trabaja el grupo estará lista “probablemente en diciembre” a un precio menor de 1.000 yuanes (144 dólares).
La vacuna se empezará a comercializar una vez termine la tercera fase de pruebas, la cual se está llevando a cabo en Emiratos Árabes Unidos, aseguró Liu en declaraciones a medios locales recogidas hoy por el periódico Global Times.
Liu agregó que el precio de esta vacuna no superará los 1.000 yuanes para las dos dosis que serán necesarias, y que la prioridad para administrarla en China serán los estudiantes y quienes trabajen en las ciudades. “No toda la población de China tendrá que vacunarse”, indicó.
Según un estudio publicado esta semana en The Journal of the American Medical Association en base a los ensayos clínicos de las fases 1 y 2, “la vacuna candidata de Sinopharm es segura y genera una respuesta inmune”, recoge la agencia estatal de noticias Xinhua.
La investigación incluye datos sobre 320 voluntarios de entre 18 y 59 años, de los cuales 96 participaron en ensayos clínicos de la fase 1 y 224 tomaron parte en la fase 2.
Los resultados mostraron que la vacuna indujo eficazmente anticuerpos neutralizantes en los voluntarios y demostró una buena inmunogenicidad, es decir la capacidad de una sustancia para desencadenar una respuesta inmune.
Sinopharm inauguró en junio un complejo farmacéutico en la ciudad de Wuhan para la investigación, el desarrollo y la producción de la vacuna con el objetivo de doblar su capacidad productiva.
El 24 de junio, la farmacéutico anunció que comenzaba la tercera fase de las pruebas clínicas en Emiratos Árabes Unidos de la posible vacuna, desarrollada conjuntamente con el Instituto de Productos Biológicos y Virología de Wuhan y la Academia China de Ciencias.
Por otra parte, la Oficina Estatal china de Propiedad Intelectual (SIPO, siglas en inglés) aprobó recientemente la primera patente de otra candidata a vacuna contra la COVID-19, también en la tercera fase de pruebas, que podría “ser producida en masa en un breve periodo de tiempo”, informó ayer la prensa local.
Esa vacuna, desarrollada por el Instituto Científico Militar y la compañía biofarmacéutica china CanSino Biologics, comenzó a usarse a finales de junio en el Ejército chino después de que un equipo dirigido por el investigador Chen Wei descubriera un anticuerpo monoclonal neutralizante altamente eficiente.
Los resultados de la segunda fase de los ensayos clínicos de la vacuna demostraron que es segura e induce respuesta inmune contra el coronavirus, de acuerdo con una investigación publicada a finales de julio en la revista The Lancet.
Según la patente de la la Oficina Estatal china de Propiedad Intelectual, la vacuna ha mostrado una “buena respuesta inmunológica en ratones y roedores, y puede inducir al cuerpo a producir una fuerte respuesta inmune celular y humoral en poco tiempo”, recoge el periódico cantonés Southern Metropolis.
La patente asegura que esta vacuna “puede ser producida en masa en un corto periodo de tiempo”, y que es “rápida y fácil de preparar”. No obstante, su seguridad y efectividad deberá confirmarse en la fase tres, que se lleva a cabo en el extranjero, agrega la información.
Hasta el momento, apunta el diario oficial China Daily, China cuenta con cinco posibles vacunas que han alcanzado al menos la segunda fase de pruebas, de las cuales una se basa en un vector viral -un adenovirus, en este caso- para transportar partes del coronavirus y las otras cuatro, en una versión inactivada del agente infeccioso causante de la pandemia de la COVID-19.
Habitualmente, el período para que una vacuna pueda estar disponible para su uso a nivel masivo es de, al menos, entre 12 y 18 meses, según la Organización Mundial de la Salud (OMS), aunque Pekín ha acelerado los procesos debido a la emergencia sanitaria y ha permitido que se lleven a cabo al mismo tiempo algunos estudios en diferentes fases.
Al respecto, González García consideró: “No me parece que tengamos una vacuna disponible antes antes de fin de año. Antes de ese tiempo puede estar aprobada en fase 3 y fabricada. Pero no creo que la tengamos disponible antes del primer trimestre”.
La importancia de estos acuerdos radica en que facilitará el acceso a dosis en el futuro.
Sin embargo, según pudo saber Infobae de parte de fuentes calificadas del Ministerio de Salud, “falta la confirmación oficial” de esos acuerdos. En la misma línea se manifestó consultado por este medio el médico infectólogo Pedro Cahn, quien aseguró que “todavía está en discusión” (que se realicen las pruebas en el país).
“En 48 horas va a haber novedades sobre las vacunas chinas”, aseveró por su parte, el ministro de Salud, Ginés González García, en declaraciones televisivas. “Estamos trabajando intensamente con China. Nosotros queremos mucho a los proveedores de vacunas; queremos que haya disponibilidad para todos los argentinos a partir de acuerdos con proveedores, sobre todo quienes están en la punta del desarrollo”, agregó.
Ayer se dio a conocer que Liu Jingzhen, el presidente de la empresa estatal China National Biotec Group, parte de la farmacéutica Sinopharm, aseguró que la vacuna contra el coronavirus en la que trabaja el grupo estará lista “probablemente en diciembre” a un precio menor de 1.000 yuanes (144 dólares).
La vacuna se empezará a comercializar una vez termine la tercera fase de pruebas, la cual se está llevando a cabo en Emiratos Árabes Unidos, aseguró Liu en declaraciones a medios locales recogidas hoy por el periódico Global Times.
Liu agregó que el precio de esta vacuna no superará los 1.000 yuanes para las dos dosis que serán necesarias, y que la prioridad para administrarla en China serán los estudiantes y quienes trabajen en las ciudades. “No toda la población de China tendrá que vacunarse”, indicó.
Según un estudio publicado esta semana en The Journal of the American Medical Association en base a los ensayos clínicos de las fases 1 y 2, “la vacuna candidata de Sinopharm es segura y genera una respuesta inmune”, recoge la agencia estatal de noticias Xinhua.
La investigación incluye datos sobre 320 voluntarios de entre 18 y 59 años, de los cuales 96 participaron en ensayos clínicos de la fase 1 y 224 tomaron parte en la fase 2.
Los resultados mostraron que la vacuna indujo eficazmente anticuerpos neutralizantes en los voluntarios y demostró una buena inmunogenicidad, es decir la capacidad de una sustancia para desencadenar una respuesta inmune.
Sinopharm inauguró en junio un complejo farmacéutico en la ciudad de Wuhan para la investigación, el desarrollo y la producción de la vacuna con el objetivo de doblar su capacidad productiva.
El 24 de junio, la farmacéutico anunció que comenzaba la tercera fase de las pruebas clínicas en Emiratos Árabes Unidos de la posible vacuna, desarrollada conjuntamente con el Instituto de Productos Biológicos y Virología de Wuhan y la Academia China de Ciencias.
Por otra parte, la Oficina Estatal china de Propiedad Intelectual (SIPO, siglas en inglés) aprobó recientemente la primera patente de otra candidata a vacuna contra la COVID-19, también en la tercera fase de pruebas, que podría “ser producida en masa en un breve periodo de tiempo”, informó ayer la prensa local.
Esa vacuna, desarrollada por el Instituto Científico Militar y la compañía biofarmacéutica china CanSino Biologics, comenzó a usarse a finales de junio en el Ejército chino después de que un equipo dirigido por el investigador Chen Wei descubriera un anticuerpo monoclonal neutralizante altamente eficiente.
Los resultados de la segunda fase de los ensayos clínicos de la vacuna demostraron que es segura e induce respuesta inmune contra el coronavirus, de acuerdo con una investigación publicada a finales de julio en la revista The Lancet.
Según la patente de la la Oficina Estatal china de Propiedad Intelectual, la vacuna ha mostrado una “buena respuesta inmunológica en ratones y roedores, y puede inducir al cuerpo a producir una fuerte respuesta inmune celular y humoral en poco tiempo”, recoge el periódico cantonés Southern Metropolis.
La patente asegura que esta vacuna “puede ser producida en masa en un corto periodo de tiempo”, y que es “rápida y fácil de preparar”. No obstante, su seguridad y efectividad deberá confirmarse en la fase tres, que se lleva a cabo en el extranjero, agrega la información.
Hasta el momento, apunta el diario oficial China Daily, China cuenta con cinco posibles vacunas que han alcanzado al menos la segunda fase de pruebas, de las cuales una se basa en un vector viral -un adenovirus, en este caso- para transportar partes del coronavirus y las otras cuatro, en una versión inactivada del agente infeccioso causante de la pandemia de la COVID-19.
Habitualmente, el período para que una vacuna pueda estar disponible para su uso a nivel masivo es de, al menos, entre 12 y 18 meses, según la Organización Mundial de la Salud (OMS), aunque Pekín ha acelerado los procesos debido a la emergencia sanitaria y ha permitido que se lleven a cabo al mismo tiempo algunos estudios en diferentes fases.
Al respecto, González García consideró: “No me parece que tengamos una vacuna disponible antes antes de fin de año. Antes de ese tiempo puede estar aprobada en fase 3 y fabricada. Pero no creo que la tengamos disponible antes del primer trimestre”.
Con información de
Infobae
Suscribite!
Y recibí las noticias más importantes!
Y recibí las noticias más importantes!
Nota22.com
LO MÁS VISTO
El regreso del método inquisitivo
El proyecto penal impulsado desde el Ministerio de Justicia y Seguridad no sólo endurece el sistema: desplaza al juez, debilita la defensa y deja decisiones graves libradas a fórmulas ambiguas.
La Superintendencia de Servicios de Salud intimó a las entidades a presentar en 15 días un programa de regularización tras detectar incumplimientos contables, financieros y prestacionales.
Distintos puntos de la ciudad capital amanecieron con carteles anónimos que mencionan al intendente de Santa Fe y hacen referencia al SEOM.
La medida fue aprobada por la Cámara de Diputados, donde se abrogó la Ley 1341, que regula los Estados de excepción

