Hito científico en la creación de órganos artificiales: por primera vez cultivaron riñones humanos en cerdos
Viernes 08 de
Septiembre 2023
Mediante la utilización de las tijeras genéticas CRISPR, investigadores lograron que los órganos contengan un 5060 % de células humanas y que, tras 28 días de gestación en ese animal, mostraran una estructura normal para su fase de desarrollo
Por primera vez, se logró cultivar riñones que contienen células humanas en embriones de cerdo, lo que significa además de una primicia mundial, un avance médico que en un futuro podría ayudar a abordar el problema de la escasez de la donación de órganos.
El descubrimiento, descrito en un estudio publicado ayer en la revista Cell Stem Cell por investigadores de los Institutos de Biomedicina y Salud de Guangzhou, en China se centró en los riñones, porque son uno de los primeros órganos en desarrollarse y los más comúnmente trasplantados en la medicina humana.
“Se han producido órganos de rata en ratones y órganos de ratón en ratas, pero los intentos anteriores de cultivar órganos humanos en cerdos no han tenido éxito. Nuestro enfoque mejora la integración de células humanas en los tejidos receptores y nos permite cultivar órganos humanos en cerdos”, dijo el autor principal Liangxue Lai en un comunicado.
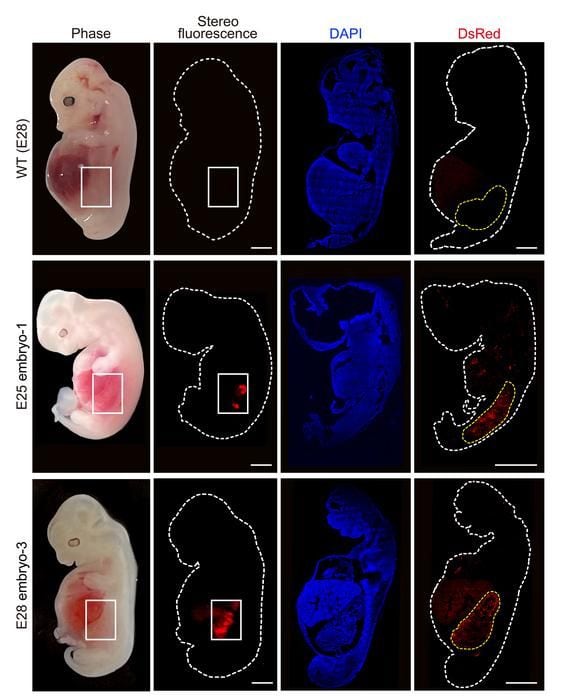
Los riñones contenían un 50–60 % de células humanas y que, tras 28 días de gestación en ese animal, mostraban una estructura normal para su fase de desarrollo. Los llamados embriones quimera contienen células de dos especies, en este caso de humano y cerdo, y es una línea de investigación en la aún lejana posibilidad de generar órganos humanos en otros animales para trasplantes.
Los expertos señalan que es la primera vez que se logra cultivar un “órgano sólido humanizado” en otra especie, aunque sí se han usado métodos similares para generar tejidos humanos como sangre o músculo esquelético en cerdos.
Paso a paso
El primer paso de los expertos fue crear un “nicho” dentro del embrión porcino para que las células humanas no tuvieran que competir con las de cerdo. Para ello, usaron la herramienta de edición genética CRISPR, con la que diseñaron un embrión unicelular porcino al que le faltaban dos genes necesarios para el desarrollo renal.
Después, diseñaron células madre pluripotentes humanas (que tienen el potencial de convertirse en cualquier tipo de célula) para hacerlas más susceptibles a la integración. Antes de implantar los embriones en desarrollo a las cerdas, los investigadores cultivaron las quimeras en condiciones optimizadas para proporcionar nutrientes y señales únicas tanto a las células humanas como a las porcinas, ya que suelen tener necesidades dispares.
Los investigadores transfirieron 1.820 embriones a 13 animales y al cabo de un periodo de entre 25 o 28 días, interrumpieron la gestación y extrajeron los embriones para evaluar si las quimeras habían logrado producir riñones humanizados.
Se analizaron cinco embriones quiméricos (dos de 25 días de implantación y tres de 28 días) en los que los riñones humanizados eran “estructuralmente normales para su fase de desarrollo y estaban compuestos por un 50-60 % de células humanas”. Los riñones estaban en la etapa de mesonefros (la segunda etapa del desarrollo renal); habían formado túbulos y brotes de células que eventualmente se convertirían en uréteres que conectarían el riñón con la vejiga.
El equipo investigó además si había células humanas en otros tejidos de los embriones, lo que podría tener implicaciones éticas, sobre todo si se encontraban abundantes células humanas en tejidos neurales o de la línea germinal y los cerdos llegaran a término.
Sin embargo, las células humanas se localizaban, sobre todo, en los riñones, mientras que el resto del embrión estaba compuesto por células porcinas. “Si se crea un nicho en el embrión porcino, las células humanas van a parar de forma natural a esos espacios”, explicó el otro autor, Zhen Dai, del Instituto de Biomedicina y Salud de Guangzhou.
Este es un enfoque diferente a los recientes avances de alto perfil en los Estados Unidos, donde se han colocado riñones de cerdo genéticamente modificados e incluso un corazón dentro de humanos. El nuevo artículo “describe pasos pioneros en un nuevo enfoque de bioingeniería de órganos utilizando cerdos como incubadoras para el crecimiento y cultivo de órganos humanos”, dijo Dusko Ilic, profesor de ciencias de células madre en el King’s College de Londres, que no participó en la investigación. Pero Ilic advirtió que habría muchos desafíos para convertir el experimento en una solución viable, pero “sin embargo, esta cautivadora estrategia merece una mayor exploración”.
Los problemas pendientes
“Sólo vimos muy pocas células neurales humanas en el cerebro y la médula espinal y ninguna célula humana en la cresta genital”. Los científicos consideran crucial impedir la invasión de células humanas en el tejido reproductivo, porque de lo contrario existe el riesgo de que se produzcan descontroladamente híbridos entre humanos y cerdos.
“La presencia de células humanas en el cerebro de los cerdos todavía genera preocupación”, dijo Darius Widera, profesor de biología de células madre en la Universidad de Reading. “Aunque este enfoque es un claro hito y el primer intento exitoso de cultivar órganos completos que contienen células humanas en cerdos, la proporción de células humanas en los riñones generados todavía no es lo suficientemente alta”, añadió.
A largo plazo, el equipo quiere optimizar su tecnología para su uso en trasplantes humanos, pero admite que aún no está lista. Una limitación importante era que los riñones tenían células vasculares derivadas de cerdos, que podían provocar rechazo si se trasplantaban a un ser humano.
Sin embargo, los científicos planean seguir adelante y permitir que los riñones se desarrollen durante más tiempo. También están trabajando en el cultivo de otros órganos humanos en cerdos, como el corazón y el páncreas. “Si se crea un nicho en el embrión porcino, las células humanas van a parar de forma natural a esos espacios”, explicó el autor principal, Zhen Dai, del Instituto de Biomedicina y Salud de Guangzhou.
El investigador aseguró que vieron “muy pocas” células neuronales humanas en el cerebro y la médula espinal y “ninguna” en la cresta genital, lo que indica que “las células madre pluripotentes humanas no se diferenciaron en células germinales”.
Este trabajo aporta “avances importantes en una de las vías que más interés ha suscitado a lo largo de los últimos años” para desarrollar un modelo de producción de órganos aptos para trasplante mediante el uso de cerdos como animal vehicular, en opinión del nefrólogo español Rafael Matesanz, ajeno al estudio.
El equipo de investigadores chinos quiere ahora permitir que los riñones humanizados se desarrollen durante más tiempo y trabajan para generar otros órganos humanos en cerdos, como el corazón y el páncreas. Aunque el objetivo a largo plazo es optimizar esta tecnología para el trasplante de órganos humanos, el equipo reconoce que el trabajo será complejo y podría llevar muchos años.
Cultivar un órgano humanizado plenamente funcional en un cerdo requeriría algunos pasos adicionales porque los órganos se componen de múltiples tipos de células y tejidos.
El descubrimiento, descrito en un estudio publicado ayer en la revista Cell Stem Cell por investigadores de los Institutos de Biomedicina y Salud de Guangzhou, en China se centró en los riñones, porque son uno de los primeros órganos en desarrollarse y los más comúnmente trasplantados en la medicina humana.
“Se han producido órganos de rata en ratones y órganos de ratón en ratas, pero los intentos anteriores de cultivar órganos humanos en cerdos no han tenido éxito. Nuestro enfoque mejora la integración de células humanas en los tejidos receptores y nos permite cultivar órganos humanos en cerdos”, dijo el autor principal Liangxue Lai en un comunicado.
Los riñones contenían un 50–60 % de células humanas y que, tras 28 días de gestación en ese animal, mostraban una estructura normal para su fase de desarrollo. Los llamados embriones quimera contienen células de dos especies, en este caso de humano y cerdo, y es una línea de investigación en la aún lejana posibilidad de generar órganos humanos en otros animales para trasplantes.
Los expertos señalan que es la primera vez que se logra cultivar un “órgano sólido humanizado” en otra especie, aunque sí se han usado métodos similares para generar tejidos humanos como sangre o músculo esquelético en cerdos.
Paso a paso
El primer paso de los expertos fue crear un “nicho” dentro del embrión porcino para que las células humanas no tuvieran que competir con las de cerdo. Para ello, usaron la herramienta de edición genética CRISPR, con la que diseñaron un embrión unicelular porcino al que le faltaban dos genes necesarios para el desarrollo renal.

Después, diseñaron células madre pluripotentes humanas (que tienen el potencial de convertirse en cualquier tipo de célula) para hacerlas más susceptibles a la integración. Antes de implantar los embriones en desarrollo a las cerdas, los investigadores cultivaron las quimeras en condiciones optimizadas para proporcionar nutrientes y señales únicas tanto a las células humanas como a las porcinas, ya que suelen tener necesidades dispares.
Los investigadores transfirieron 1.820 embriones a 13 animales y al cabo de un periodo de entre 25 o 28 días, interrumpieron la gestación y extrajeron los embriones para evaluar si las quimeras habían logrado producir riñones humanizados.
Se analizaron cinco embriones quiméricos (dos de 25 días de implantación y tres de 28 días) en los que los riñones humanizados eran “estructuralmente normales para su fase de desarrollo y estaban compuestos por un 50-60 % de células humanas”. Los riñones estaban en la etapa de mesonefros (la segunda etapa del desarrollo renal); habían formado túbulos y brotes de células que eventualmente se convertirían en uréteres que conectarían el riñón con la vejiga.
El equipo investigó además si había células humanas en otros tejidos de los embriones, lo que podría tener implicaciones éticas, sobre todo si se encontraban abundantes células humanas en tejidos neurales o de la línea germinal y los cerdos llegaran a término.
Sin embargo, las células humanas se localizaban, sobre todo, en los riñones, mientras que el resto del embrión estaba compuesto por células porcinas. “Si se crea un nicho en el embrión porcino, las células humanas van a parar de forma natural a esos espacios”, explicó el otro autor, Zhen Dai, del Instituto de Biomedicina y Salud de Guangzhou.
Este es un enfoque diferente a los recientes avances de alto perfil en los Estados Unidos, donde se han colocado riñones de cerdo genéticamente modificados e incluso un corazón dentro de humanos. El nuevo artículo “describe pasos pioneros en un nuevo enfoque de bioingeniería de órganos utilizando cerdos como incubadoras para el crecimiento y cultivo de órganos humanos”, dijo Dusko Ilic, profesor de ciencias de células madre en el King’s College de Londres, que no participó en la investigación. Pero Ilic advirtió que habría muchos desafíos para convertir el experimento en una solución viable, pero “sin embargo, esta cautivadora estrategia merece una mayor exploración”.
Los problemas pendientes
“Sólo vimos muy pocas células neurales humanas en el cerebro y la médula espinal y ninguna célula humana en la cresta genital”. Los científicos consideran crucial impedir la invasión de células humanas en el tejido reproductivo, porque de lo contrario existe el riesgo de que se produzcan descontroladamente híbridos entre humanos y cerdos.
“La presencia de células humanas en el cerebro de los cerdos todavía genera preocupación”, dijo Darius Widera, profesor de biología de células madre en la Universidad de Reading. “Aunque este enfoque es un claro hito y el primer intento exitoso de cultivar órganos completos que contienen células humanas en cerdos, la proporción de células humanas en los riñones generados todavía no es lo suficientemente alta”, añadió.
A largo plazo, el equipo quiere optimizar su tecnología para su uso en trasplantes humanos, pero admite que aún no está lista. Una limitación importante era que los riñones tenían células vasculares derivadas de cerdos, que podían provocar rechazo si se trasplantaban a un ser humano.
Sin embargo, los científicos planean seguir adelante y permitir que los riñones se desarrollen durante más tiempo. También están trabajando en el cultivo de otros órganos humanos en cerdos, como el corazón y el páncreas. “Si se crea un nicho en el embrión porcino, las células humanas van a parar de forma natural a esos espacios”, explicó el autor principal, Zhen Dai, del Instituto de Biomedicina y Salud de Guangzhou.
El investigador aseguró que vieron “muy pocas” células neuronales humanas en el cerebro y la médula espinal y “ninguna” en la cresta genital, lo que indica que “las células madre pluripotentes humanas no se diferenciaron en células germinales”.
Este trabajo aporta “avances importantes en una de las vías que más interés ha suscitado a lo largo de los últimos años” para desarrollar un modelo de producción de órganos aptos para trasplante mediante el uso de cerdos como animal vehicular, en opinión del nefrólogo español Rafael Matesanz, ajeno al estudio.
El equipo de investigadores chinos quiere ahora permitir que los riñones humanizados se desarrollen durante más tiempo y trabajan para generar otros órganos humanos en cerdos, como el corazón y el páncreas. Aunque el objetivo a largo plazo es optimizar esta tecnología para el trasplante de órganos humanos, el equipo reconoce que el trabajo será complejo y podría llevar muchos años.
Cultivar un órgano humanizado plenamente funcional en un cerdo requeriría algunos pasos adicionales porque los órganos se componen de múltiples tipos de células y tejidos.
Con información de
Infobae
YPF confirmó un nuevo aumento en los combustibles: de cuánto es y qué pasará con el congelamiento
El anuncio lo realizó Horacio Marín. Además, la suba rige a partir de este jueves.
Sorpresa: una encuesta midió a Victoria Villarruel como variante del PRO y el PJ para 2027
Lo hizo DC Consultores en su último estudio nacional. Es una firma que suele darle buenos números al Gobierno. Además, ranking de imágenes con 9 dirigentes y outsiders.
Hoy se conocerá la inflación de abril: el Gobierno anticipó una baja fuerte y busca consolidar la desaceleración
Las proyecciones privadas y del ministro de Economía, Luis Caputo, coinciden en que el Índice de Precios al Consumidor (IPC) mostrará una disminución respecto a marzo. Cómo viene mayo y las medidas con los servicios públicos
Suscribite!
Y recibí las noticias más importantes!
Y recibí las noticias más importantes!
Nota22.com
Crecen las críticas a la gestión del Intendente de Santa Fe, Juan Pablo Poletti
LO MÁS VISTO
El bullying y los derechos humanos
¿Que es el Bullying?
El Juzgado de 1ra. Instancia en lo Civil y Comercial de la Octava Nominación falló a favor de la Municipalidad de Sauce Viejo en medio del conflicto que mantiene con la Asociación de Obreros y Empleados Municipales.
Lo anticipó el ministro Mario Lugones en una jornada sobre salud en la que se alertó sobre la creciente judicialización del sistema. El objetivo del Gobierno es que cualquier médico no pueda recetar cualquier tipo de medicamento y ajustan detalles de la norma.
El exministro de Economía le respondió al Presidente a través de una publicación en su blog personal; "Me limité a repetir lo que él mismo había dicho", manifestó




